Kjeldahl Stickstoffbestimmung
Ablauf der Stickstoff-/Proteinbestimmung nach Kjeldahl
Das Kjeldahl-Verfahren ist eine anerkannte Methode, die breite Anwendung bei allen Arten von Lebensmittelproben findet, aber auch bei chemischen, pharmazeutischen und Umweltproben verwendet wird. Dabei werden in einem Aufschlussschritt Proteine und andere stickstoffhaltige Spezies zersetzt und anschliessend mittels Dampfdestillation das Ammoniak zur Stickstoffquantifizierung isoliert.

Das Kjeldahl-Verfahren
Proteine zählen zu den wichtigsten Nahrungsmittelbestandteilen und sind in nahezu allen Lebens- und Futtermitteln enthalten, wo sie als zuverlässiger Qualitätsparameter dienen. Bei Lebensmitteln muss der Proteingehalt in den Nährwertangaben für Konsumenten angegeben werden. Diese Angabe ist für Lebensmittelhersteller sowohl im Rahmen der nationalen als auch der internationalen Gesetzgebung vorgeschrieben. Bei Bestimmung des gesamten Kjeldahl-Stickstoffs (TKN) lässt sich der Proteingehalt unmittelbar aus dem Stickstoffgehalt der Probe berechnen. Mit der TKN-Analyse lässt sich auch der Gehalt an sowohl organischen als auch anorganischen Stickstoffformen in den betreffenden Proben ermitteln, und sie ist für viele Anwendungen nutzbar. Bei der Lebensmittelanalyse wird der gesamte flüchtige basische Stickstoff (TVBN) zur Bestimmung des Frischegrads von Fisch und Meeresfrüchten herangezogen.

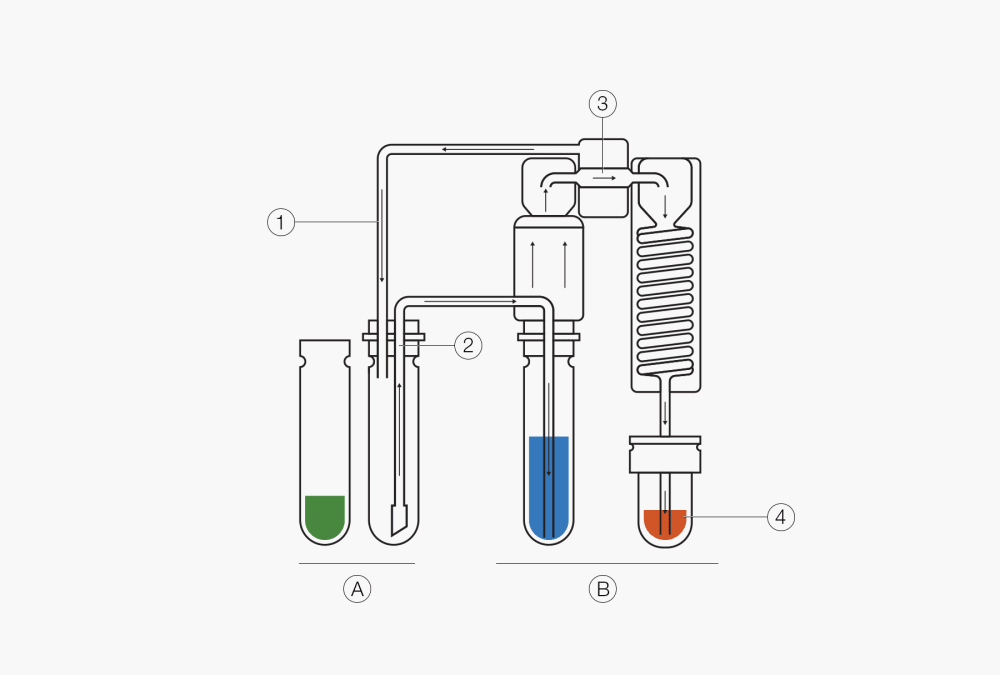
Abb. 1 Die drei Hauptschritte der Kjeldahl-Stickstoffbestimmung umfassen Aufschluss, Dampfdestillation und Titration.
Schritt 1: Aufschluss
Die Analyse beginnt mit dem Säureaufschluss der Probe unter Einsatz eines Digesters, wobei organischer Stickstoff zu Ammoniak umgewandelt wird. Die Probe muss in konzentrierter Schwefelsäure mit kaliumsulfathaltigen Kjeldahl-Tabletten und einem Kupferkatalysator sieden, um den organischen Stickstoff zu Ammoniak umzuwandeln (Abb. 2). Der Digester ist an einen Scrubber gekoppelt, um korrosive Dämpfe zu entfernen und damit höchste Laborsicherheit zu erzielen.
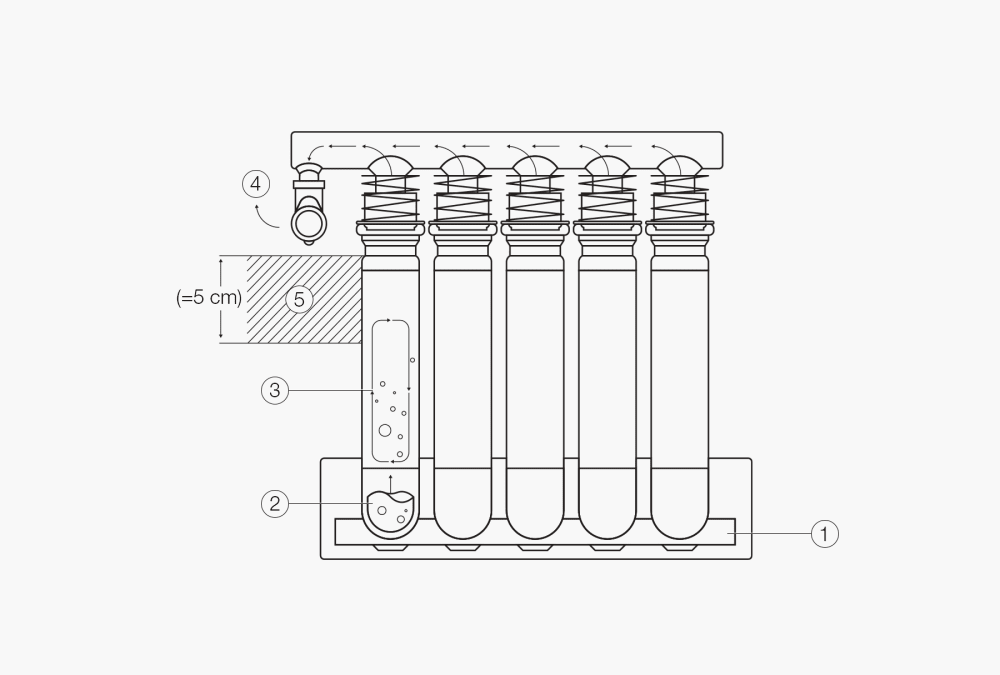
Abb. 2 Das Aufschlussverfahren mittels Blockheizung.
Der Aluminiumblock ① generiert hohe Temperaturen in den Proben ②
Die Probe wird in konstant siedender Schwefelsäure aufgeschlossen
Heisse Säuredämpfe steigen in die Kondensationszone ③ auf, kondensieren und laufen wieder in die Probe zurück, wodurch ein konstanter Rückfluss entsteht
Restdämpfe ④, die aus der Kondensationszone ⑤ entweichen, sind äusserst korrosiv und müssen abgezogen und wirksam neutralisiert werden (z. B. mit dem Scrubber K-415)
Schritt 2: Das Dampfdestillationsverfahren und die Titration
Der zweite Teil der Methode umfasst eine Dampfdestillation mit einem geeigneten Destillationsgerät. Der pH-Wert des Gärrests muss bei diesem Alkalisierungsschritt durch Zusetzen von konzentriertem Natriumhydroxid auf 9.5 gebracht werden. Bei diesem pH-Wert bildet sich Ammoniakgas. Mit dem Reaktionserkennungssensor wird automatisch die Menge an Natriumhydroxid optimiert, was Ressourcen und Kosten einspart. Das Ammoniakgas wird dann mittels Dampfdestillation in die saure Absorptionslösung, nämlich verdünnte Borsäure, überführt und in Ammonium umgewandelt (Abb. 3). Die Stickstoffkonzentrationen in der Empfängerlösung können dann mit Hilfe der klassischen potentiometrischen oder kolorimetrischen Elektrodenbestimmungsmethoden ermittelt werden.