Lyophilisation
Présentation du processus de lyophilisation
La lyophilisation est le procédé le moins destructeur pour sécher différents types de matières périssables. Le principe de la lyophilisation repose sur le passage direct de l’état solide à l’état gazeux, un phénomène appelé « sublimation ». Le produit est d’abord congelé, puis séché par sublimation dans un environnement à basse pression.
Avantages du processus de lyophilisation
La réduction de la teneur en eau augmente fortement la stabilité du produit en raison du lien direct entre la présence d’eau et les activités biologique et chimique en grande partie responsables de sa dégradation. Par rapport à d’autres méthodes de déshydratation, la lyophilisation endommage moins le produit et évite le rétrécissement ou l’agglomération de la matière. De ce fait, la méthode de lyophilisation est idéale pour :
- la préservation de matières délicates contre la dégradation ou la décomposition
- la protection des caractéristiques et de la forme initiale des produits
- la conservation de produits qui nécessitent une réhydratation rapide ou le conditionnement pour un usage ultérieur
Le processus de congélation initial entraîne la formation de cristaux de glace à l’intérieur du produit et à sa surface. En se transformant en glace, chaque molécule d’eau est piégée dans une architecture bien définie. Au moment de la sublimation, elles laissent de petits pores et des interstices dans le produit qui conserve alors sa forme et sa structure. La réhydratation du produit est alors simple et rapide, ce qui est particulièrement important dans les applications pharmaceutiques. Les produits lyophilisés peuvent se conserver plusieurs années à température ambiante s’ils sont bien protégés contre l’humidité et l’oxygène dans un emballage scellé.
Les vaccins, les fruits et légumes secs, les champignons déshydratés et le café soluble sont des produits lyophilisés courants de la vie quotidienne.
Principe du processus de lyophilisation : bases de la thermodynamique
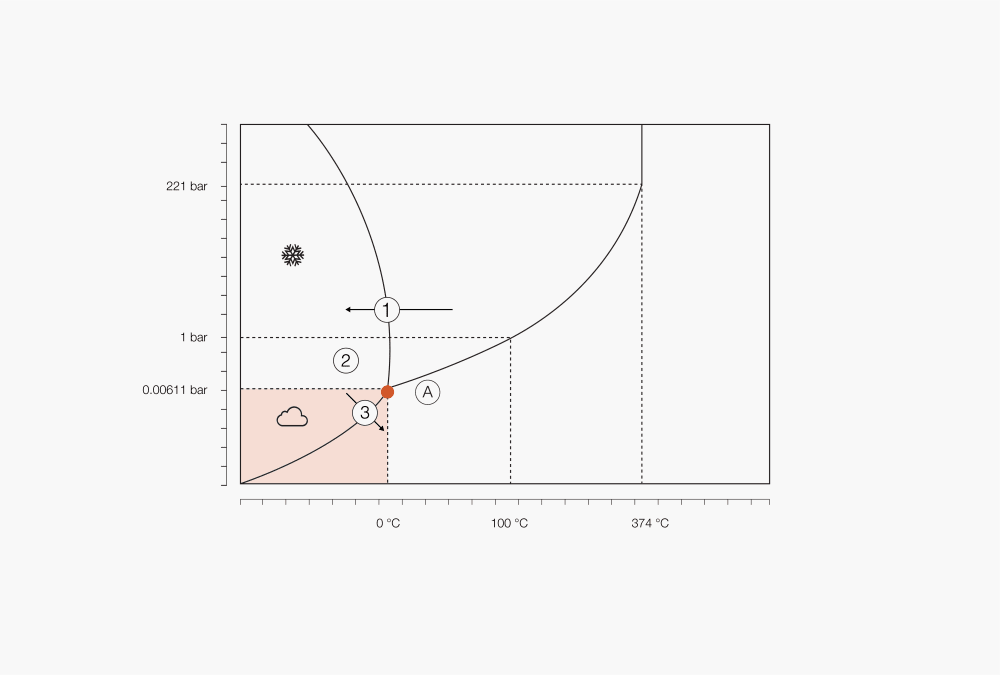
Figure 1 : Diagramme de phase de l’eau
① Choix de la température de congélation en fonction des solvants et du soluté
② Début de la sublimation en abaissant la pression
③ Démarrage de la lyophilisation en dessous du point triple
Ⓐ Point triple
En fonction de la pression et de la température, n’importe quelle substance peut être présente sous trois phases : solide, liquide et gazeuse. Pour chaque substance, la relation entre la pression et la température peut être représentée dans un « diagramme de phase ». Lorsqu’un solide est chauffé sous pression constante au- dessus du point triple, il atteint le point de fusion et se liquéfie. Si le chauffage est prolongé, la température augmente jusqu’au point d’ébullition. Le liquide commence alors à bouillir et se transforme en gaz.
Lorsque le même processus est effectué à une température et une pression inférieure au point triple (pour l’eau, 6,11 mbar), la matière subit une sublimation plutôt que de passer par la fusion. La chaleur appliquée sous basse pression à l’échantillon transfère suffisamment d’énergie pour provoquer sa décongélation, mais puisque la pression est trop faible pour la formation de liquide, le solvant se sublime en gaz.
La phase de la substance étant déterminée à la fois par la chaleur et la pression, les températures d’ébullition et de vaporisation dépendent de la pression. La diminution de la pression par l’application de vide peut donc entraîner l’abaissement du point d’ébullition du solvant et la vaporisation à des températures plus basses. Les systèmes à basse pression sont généralement utilisés lors du traitement d’échantillons thermosensibles pour abaisser le point d’ébullition et ainsi provoquer la vaporisation à une température inférieure moins destructive. Une approche similaire peut être adoptée pour les procédés de sublimation.
Effets de la pression et de la température sur la méthode de lyophilisation

Figure 2 : Étapes de la lyophilisation
■ Pression
■ Produit
■ Plateau
■ Condenseur
Ⓐ La diminution de la température du produit et du plateau permettent un processus optimal
Ⓑ La diminution de la pression et l’augmentation de la température du plateau facilitent la sublimation ainsi que la désorption dans l’étape de dessiccation secondaire
Ⓒ La température du cryocondenseur détermine la capacité réelle du condenseur pour recueillir les vapeurs
Les paramètres cruciaux régissant votre équipement de lyophilisation sont la pression et la température.Typiquement, le processus de lyophilisation comporte deux étapes : la congélation et la dessiccation primaire. Avec certains échantillons, une étape de dessiccation secondaire peut s’avérer nécessaire pour éliminer les molécules de solvant fortement imbriquées et abaisser encore le taux d’humidité. Selon les caractéristiques de l’échantillon, chaque étape du processus possède des exigences propres en matière de pression et de température.
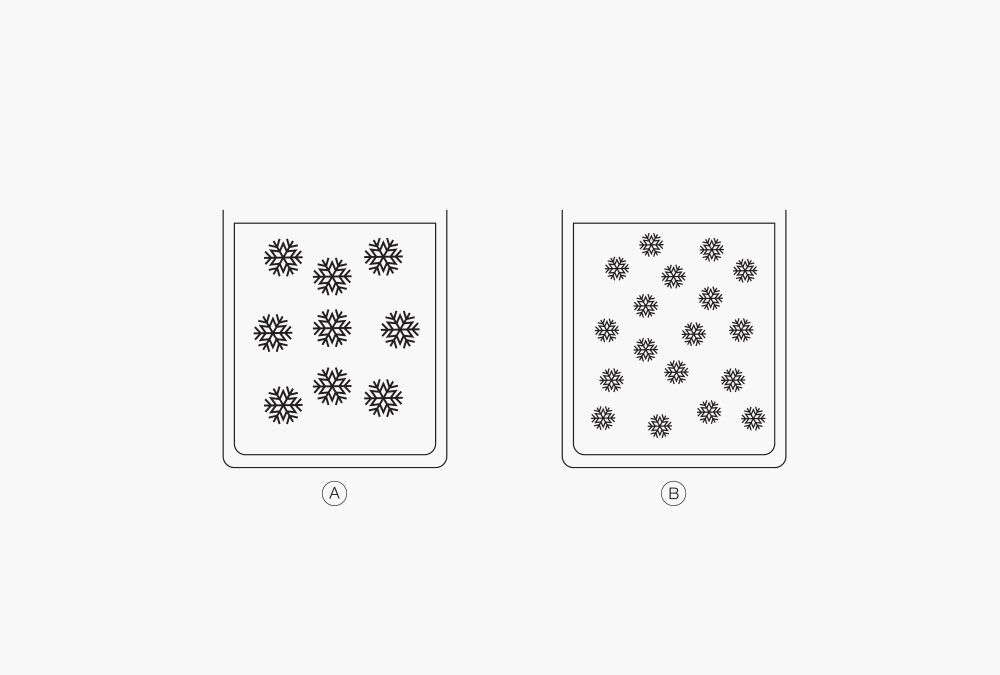
Figure 3: La taille des cristaux de glace varie en fonction de la vitesse de congélation
Ⓐ Congélation lente
Ⓑ Congélation rapid
La plupart des produits liquides – ou formulations – génèrent des cristaux de glace en gelant. La taille et la forme des cristaux de glace dépendent de la vitesse de refroidissement, et elles déterminent l’aptitude à la lyophilisation. Les cristaux de glace sont plus petits avec un refroidissement rapide (à l’azote liquide) et plus gros avec un refroidissement plus lent (surgélation). En ce qui concerne la lyophilisation, les petits cristaux de glace sont plus difficiles à éliminer du produit que les gros.Cependant, la température de congélation d’une formulation est définie par ses caractéristiques et sa composition.
Mélanges eutectiques et amorphes dans le processus de lyophilisation
Généralement, les formulations peuvent être congelées de deux manières pour les mélanges eutectiques et amorphes.
Mélanges eutectiques
Les mélanges eutectiques contiennent des substances gelant à des températures inférieures à l’eau qui les entoure. Lors du refroidissement d’un mélange eutectique, l’eau est la première à se séparer des substances et elle se transforme en glace. La formulation peut alors sembler gelée, mais les substances restantes sont en fait toujours liquides. Elles forment des zones concentrées qui finissent par geler à des températures inférieures au point de congélation de l’eau.
La température à laquelle tous les composants du mélange sont effectivement gelés est appelée « température eutectique ». Il s’agit de la température critique de la formulation, celle qui peut être supportée au maximum pendant la lyophilisation. L’application de vide à un mélange eutectique incomplètement congelé peut entraîner la destruction du produit, car les composants non congelés se dilatent lorsqu’ils sont mis sous vide.
Mélanges amorphes
Dans l’autre catégorie de mélanges, dits « amorphes », la congélation provoque la formation d’états vitreux. À mesure que la température diminue, la formulation devient de plus en plus visqueuse et finit par se figer en un solide vitreux au point de transition vitreuse. Pour les produits amorphes, le point critique de stabilité est appelé « température d’effondrement ». En règle générale, il est quelque peu inférieur au point de transition vitreuse. Les produits amorphes sont généralement très difficiles à lyophiliser à l’aide d’un équipement de lyophilisation.
Dessiccation primaire pendant la méthode de lyophilisation
La première phase de dessiccation, dite « primaire », élimine la majeure partie de l’eau contenue dans le produit par sublimation. La température du produit est définie par la pression dans la chambre de séchage, et l’apport de chaleur doit être soigneusement contrôlé. Idéalement, la température du produit doit être la plus élevée possible pour maximiser la différence de pression de vapeur entre l’échantillon et le condenseur. Cependant, elle doit rester inférieure à la température critique du produit afin de permettre la congélation. Au-delà de cette température, la structure du produit s’effondre, ce qui entraîne des rétrécissements ou des fissures.
Dans des conditions optimales, le processus de lyophilisation s’effectue à des températures tout juste inférieures à la température critique. L’étape principale du processus de lyophilisation se déroule comme suit:
- Dans la chambre de séchage, la pression est réduite pour activer la dessiccation
- La pression et la température dominantes sont alors toutes deux inférieures au point triple
- L’utilisation de plateaux chauffants permet de s’approcher lentement de la température de consigne à un rythme prédéfini
- La sublimation crée de la vapeur d’eau dans la chambre de séchage
- Si elle n’est pas retirée du système, la vapeur d’eau s’équilibre et la sublimation des particules de glace cesse
- Les particules de vapeur sont éliminées au moyen d’un cryocondenseur, un dispositif de refroidissement qui génère des températures très inférieures à la température critique du produit
Pour l’essentiel, la vitesse de sublimation est définie par la différence des pressions de vapeur : la pression de la vapeur sur le produit d’une part, et la pression de la vapeur sur le cryocondenseur d’autre part. En général, plus la différence est grande, plus la sublimation est rapide. Et plus la température du produit est proche du point triple, plus la différence de pression est importante.
La grande majorité de l’eau doit être éliminée à la fin de la phase de dessiccation primaire par l’équipement de lyophilisation. La teneur en humidité résiduelle du produit peut maintenant être de 5-10 % en raison de l’eau liée à la matrice. À ce stade, il ne devrait plus y avoir de glace.
Dessiccation secondaire pendant le processus de lyophilisation
L’étape de dessiccation secondaire élimine les molécules d’eau adsorbées par désorption. Pour obtenir des conditions idéales de désorption, la pression la plus faible possible ainsi qu’une nouvelle hausse de la température du plateau sont nécessaires. À nouveau, la stabilité du produit doit être prise en compte au moment de choisir la température du plateau. La durée de la phase de dessiccation secondaire est généralement plus courte. Lorsque cette phase s’achève, la teneur en humidité du produit doit être comprise entre 1 et 5 %.
Le processus de lyophilisation dans l’industrie pharmaceutique
Le processus de lyophilisation est généralement la méthode privilégiée pour conserver de nombreux types de produits pharmaceutiques, surtout si la stabilité à l’état liquide n’est pas optimale, si les conditions de conservation sont trop rigoureuses ou si le produit doit se présenter sous forme solide.Elle est bien adaptée aux formulations qui n’ont besoin d’aucun traitement supplémentaire après la dessiccation et qui peuvent être conditionnées directement dans des flacons scellés juste après le cycle pour éviter les contaminations potentielles.
| Avantages de la lyophilisation | Limites de la lyophilisation |
|---|---|
Températures de traitement basses | Nécessite un investissement initial important pour l’équipement de lyophilisation |
Rendements des produits élevés | Temps de traitement longs |
Excellente uniformité des produits | Possibilités de mise à l’échelle limitées |
Grande qualité en matière d’activité, de teneur en eau et de stabilité |
|
Un contrôle précis du processus permet d’obtenir des produits de la plus haute qualité, car il aide à limiter le dépassement des propriétés intrinsèques telles que les températures d’effondrement, de fusion eutectique et de transition vitreuse.
